前言:一代EGFR-TKI的术后辅助治疗经历了两个研究高潮,第一个高潮出现在2005年左右,包括RADIANT研究及BR19研究陆续启动;第二个研究高潮出现在2011年左右,包括ADJUVANT研究及EVAN研究等陆续启动。如今,经过10余年的随访,这些研究的长期随访数据已经陆续公布,而研究结果却“互相拆台”。一代EGFR-TKI在术后辅助治疗到底有何地位。本期推送,小张结合今年ASCO的几项相关研究,系统整理术后辅助靶向治疗的研究进展,并简单分析一下这一领域目前的一些问题。
一、以RADIANT及BR19研究为代表的第一个高潮早在2002年,易瑞沙尚未上市的时候,将易瑞沙应用于术后辅治疗领域的III期临床研究——BR19研究就已经开启。研究计划入组1242例术后切除的Ib-IIIa期患者。无论是否携带EGFR基因突变,均允许患者入组。但前503例患者入组后,因无效性分析,研究被提前关闭。经过中位4.7年的随访后,并未发现吉非替尼术后辅助治疗可以改善患者的OS(HR=1.24)或DFS(HR=1.22)。
4年后的2006年,在首款EGFR-TKI上市后的第3年,第二个靶向辅助治疗的研究——RADIANT研究开启。这项研究共纳入937例术后切除的Ib-IIIa期NSCLC患者,随机接受厄洛替尼或安慰剂治疗2年,主要研究终点是DFS。虽然该研究已经有意识的筛选患者,但由于当时IPASS研究数据尚未公布,EGFR突变类型与一代EGFR-TKI疗效的关系尚不明确,因此,研究错误的以EGFR蛋白过表达和基因扩增(FISH方法检测)作为入组标准。两组之间的DFS分别为50.5个月和48.2个月。不过这个研究中,研究者将EGFR突变患者的DFS和OS设定为关键次要研究终点,共计161例(16.5%)患者,两组中位DFS分别为46.4个月和28.5个月(P=0.039),但由于续贯传递的原因,未达到统计学显著性。
2008年1月,第三项术后辅助治疗的研究—SELECT研究启动,与RADIANT研究及BR19研究最大的不同是,该研究以EGFR突变作为入组条件,精准的选对了人群,但该研究有两个很大的缺点:允许Ia期患者入组、单臂设计。最终数据分析时,13%的Ia期患者纳入研究中,经过中位5.2年的随访后,全组患者的2年DFS率为88%,5年OS率为86%,与历史对照相比均有提高。虽然单臂研究结果并未使得一代EGFR-TKI获得相应的适应症,但却提示我们:如果选对了合适的人群,或许TKI的术后辅助治疗会有一片新天地。由此,为第二次研究高潮的到来奠定基础。
关于IPASS研究的“前世今生”,相信肺癌领域的研究同行对这个故事已经非常熟悉。该研究最大的意义就是明确了EGFR突变类型与一代EGFR-TKI疗效的关系,从此,临床上均是以EGFR突变,而非蛋白过表达或基因扩增进行人群的筛选。初步扫清了“人群选择”这一障碍后,术后辅助靶向治疗迎来了第二个研究高潮。三、以ADJUVANT和EVAN等研究为代表的第二个研究高潮2011年左右,ADJUVANT、EVAN、EVIDNECE及IMPACT等四项研究陆续启动,旨在探索一代EGFR-TKI术后辅助治疗的疗效及安全性;同时,旨在探索治疗时长(1年vs.2年)的ICOMPARE研究同时启动。即同一时间段内,几乎有5项研究同时展开。ADJUVANT研究(吉非替尼2年治疗,纳入N1-N2的患者)首次分析的DFS数据和最终分析的OS数据分别发表于LancetOncology和Journalof Clinical Oncology杂志。一代EGFR-TKI和4周期含铂双药化疗的DFS分别为28.7个月和18.0个月(HR=0.60,P=0.0054),但去年公布的OS却是阴性的结果,两组中位OS分别为75.5个月和62.8个月(HR=0.92;P=0.674)。ADJUVANT研究得到了DFS阳性,但OS是阴性的结果。
EVAN研究(厄洛替尼2年治疗,仅纳入IIIa期患者)首次分析数据发表于 Lancet RespiratoryMedicine,2年的厄洛替尼和化疗的中位DFS分别为42.4个月和21.0个月(HR=0.268,P<0.001),今年ASCO年会,EVAN研究公布了最终的OS数据,两组的中位OS分别为84.2个月和61.1个月,5年OS率分别为84.8%和51.1%(HR=0.318)。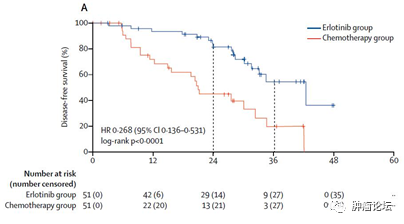
IMPACT研究(吉非替尼2年治疗,纳入II-III期患者)是由日本学者发起,本届ASCO年会以口头汇报的形式公布(摘要号:8501),经过中位71个月的随访后,靶向治疗组和化疗组的中位DFS分别为36个月和25.2个月,但差异无统计学意义(HR=0.92,P=0.63),两组的OS同样无差异,5年OS率分别为78%和74.6%,差异无统计学意义(HR=1.03,P=0.89)。
EVIDENCE研究(埃克替尼2年治疗,II-IIIa期患者)的研究数据于去年世界肺癌大会公布,两组的中位DFS分别为46.95个月和22.11个月,差异有统计学意义(HR=0.36,P<0.001)。
ICOMPARE研究则率先比较了埃克替尼的治疗时长(1年vs. 2年)对疗效的影响。这项II期临床研究共纳入109例患者,接受1年和2年埃克替尼治疗的患者,中位DFS分别为48.92个月和32.89个月,差异有统计学意义(HR=0.521,P=0.039)。在术后辅助治疗领域,有两个关键的问题需要搞清楚:治疗谁?治疗时长?治疗谁,本质问题就是人群的选择问题。从现在的循证医学证据来看,把II-IIIa期患者纳入研究,得到的DFS是有争议的,在治疗2年的情况下,ADJUVANT研究和EVIDENCE研究得到的是阳性结果,但IMPACT研究则是阴性结果;而从OS角度来看,目前已经揭晓的ADJUVANT研究和IMPACT研究均是阴性结果,而EVIDENCE研究虽然在首次数据公布的时候并未展示OS数据,但两条生存曲线已经开始出现融合的趋势,与当年的ADJUVANT研究的首次数据分析时颇有相似之处;而如果把研究人群进一步限定在N2的患者,结果同样存在争议。在EVAN研究中,患者接受2年厄洛替尼得到的是阳性结果,而在ADJUVANT研究的亚组分析中,N2的患者两组之间的OS无差异,HR=0.92,与N1患者的0.97基本不存在任何区别。而且需要注意的是,EVAN研究虽然是阳性结果,但是,该研究的主要研究终点是2年的DFS率,而不是DFS或者OS,因此,该研究OS的阳性结果本质上仍然是探索性的而不是确认性的。因此,即使针对N2的患者进行分析,有限的探索性数据得到的结论仍然是互相拆台。
目前,术后辅助治疗的人群选择都是基于TNM分期,但是,TNM分期是一个及其宏观的预后模型,因为对于术后的患者,TNM分期主要纳入了两个参数——肿瘤直径和淋巴结转移状态,这显然是不够的。因此,第二轮研究高潮虽然得到DFS阳性结果,但OS基本都是阴性结果,本质原因和第一轮是一样的——人群的选择仍然不足够精准。关于术后复发因素的研究,除了已经纳入TMN分期中的几个因素外,很多因素均与预后有关,而目前研究较为充分的是病理亚型——实体和微乳头的患者预后更差。基于此选择病人可以将研究人群的选择由宏观水平转入组织病理水平。而进一步,通过微小残留病灶的检测,识别复发高危人群,并针对性的给予治疗,能否使人群选择更加精准,从而将隐匿性转移病灶清除,将可能复发的患者转变为不复发患者,从而得到OS的改善呢?其实,关于肺癌的术后管理,目前仍然比较“粗糙”,甚至我们连最起码的复发风险分层都没有。小张相信,一旦肺癌的术后复发风险有一个公认的、得到临床验证的且足够精准的模型后,肺癌的术后辅助靶向治疗会再次迎来新的高潮。关于治疗时长,我们目前只知道给予1年的治疗尚且不够,延长至2年可以进一步给患者带来获益。但是,在2年基础上进一步延长治疗时间,能否给患者带来进一步获益呢?目前尚无数据证明这一问题。当2年的治疗OS是阴性结果,而最佳治疗时间又不明确的时候,是否停药就成了临床很纠结的问题。在ADJUVANT研究首次公布的时候,LancetOncology曾经发表过一篇评论,评论的最后一句话小张很认可:要么不进行术后辅助靶向治疗,要么治疗开始后就不要终止。
小结:关于术后辅助治疗我们虽然有了众多的循证医学证据,但关键和核心的问题仍然没有回答。对II-IIIa期患者,无差别的均基于2年的靶向疗合适吗?不明确,因为DFS的结果有争议,OS结果不获益;对于高危的N2患者,给予靶向治疗有获益吗?不清楚,因为仅有的数据得到完全相反的结论;2年后延长治疗时间有获益吗?不明确,因为没有这方面的数据。我们知道的更多,所以我们知道的更少。小张认为,虽然目前很多关键的问题尚未得到肯定的答案,这些术研究的意义在于,对于那些不想化疗的患者,你可以理直气壮的说一声:那就吃靶向吧,效果最起码也不差。这为临床提供了一个可选择的策略。





















 010-82736610
010-82736610
 股票代码: 872612
股票代码: 872612
 京公网安备 11010802020745号
京公网安备 11010802020745号










