
铁死亡可以作为杀死间充质状态细胞的新型细胞死亡或作为免疫疗法和化学疗法的重要协同剂。
作为新的细胞死亡机制,铁死亡是近几年来的研究热点,可能参与癌细胞死亡、神经毒性、神经退行性疾病、急性肾 功能衰竭、药物性肝毒性、肝脏和心脏缺血/再灌注损伤和T细胞免疫等生命过程。
有关研究表明:通过激活或抑制铁死亡可以干预疾病的发展,因此通过对影响铁死亡的相关基因整理,探讨铁死亡在各类疾病中发挥的作用,对于人类疾病的临床治疗具有重要的现实意义。
01.研究背景
铁死亡是铁和活性氧(ROS)依赖性的调节性细胞死亡形式,是不同于细胞凋亡、细胞坏死、细胞自噬的新型细胞死亡方式。与其他细胞死亡的形态学特征不同,铁死亡存在比正常线粒体更小的线粒体,且具有线粒体膜密度浓缩、线粒体嵴减少或消失以及线粒体外膜破裂等特征(表1)。
 (表1)
(表1)
02.铁死亡发生机制
铁死亡的发生是细胞内脂质活性氧(ROS)生成与降解的平衡失调所致。铁死亡诱导剂通过不同的通路直接或间接作用于谷胱甘肽过氧化物酶(GPXs),导致细胞抗氧化能力降低,ROS 堆积,最终引起细胞氧化性死亡。
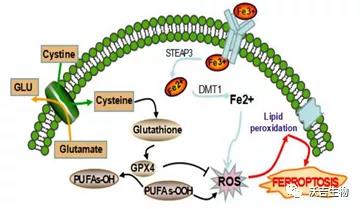
03.铁死亡调控网络
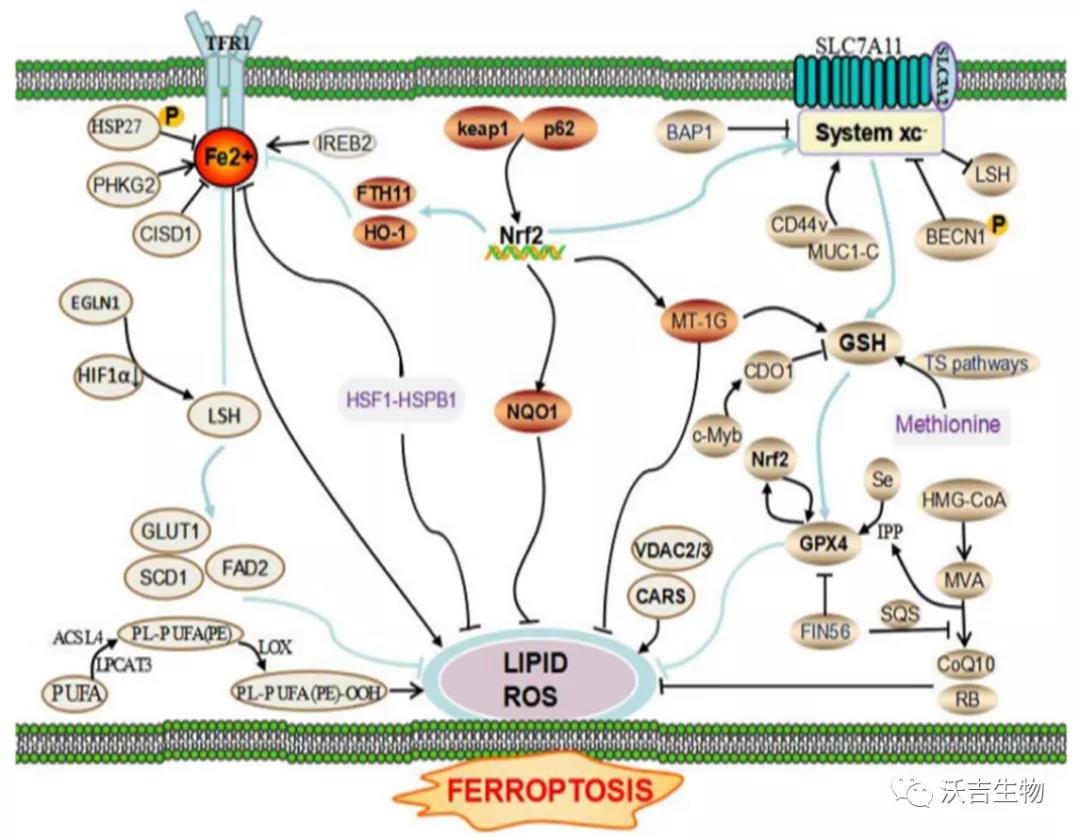
铁死亡的调节网络:PHKG2、IREB2和CISD1它们在铁代谢平衡中的功能在铁死亡中发挥重要作用。HSP27通过磷酸化阻断细胞骨架介导的铁吸收来诱导铁死亡抗性。EGLN1可以通过限制HIF 1α 上调 LSH 表达。LSH 通过影响代谢相关基因(包括SCD1、GLUT1和FADS2)来抑制铁死亡。此外,蛋白激酶C介导的 HSPB1 是铁死亡的负调节因子,通过抑制 ROS 产生和减少铁摄取。p62-Keap1-Nrf2 通路通过调节Nrf2靶向基因HO-1、FTH1和NQO1,在对抗铁死亡中发挥重要作用。AMPK介导的BECN1磷酸化和BAP1直接抑制System xc-活性,导致ROS水平升高和铁死亡。MUC1-C 与 CD44v 结合促进System xc - 的稳定性。CDO1 的抑制恢复 GSH 的水平并增加 ROS。甲硫氨酸可以通过硫转移途径转化为 腺苷同型半胱氨酸 和 Cys,这是GPX4生物合成所必需的。IPP和CoQ10是MVA途径的重要产物,促进GPX4的合成。FIN56 处理还通过调节 SQS 来减少CoQ10。VDAC2/3 和 CARS 是铁死亡的正调节因子。ROS积累需要ACSL4 和 LPCAT3 激活 PUFA。而LOX直接催化磷脂PUFAs的过氧化。
04.研究前景
铁死亡调节也涉及其他类型的 RCD。因此,铁死亡研究中最重要的目标是确定铁依赖性 ROS 代谢的下游信号通路或执行者,以将铁死亡与其他类型的 RCD 区分开来。
Ras 依赖性和非依赖性方式,表明癌细胞在铁死亡反应的时间中表现出遗传异质性。进一步定义癌症中铁死亡的基因型选择性活性以及所涉及的机制,对于指导基于铁死亡的治疗干预非常重要。铁死亡为抗肿瘤治疗提供一种新方法,目前的研究主要集中在消灭残余或耐药性癌细胞上。
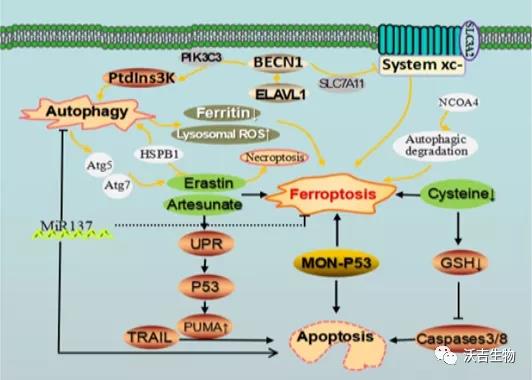
癌症中铁死亡、细胞凋亡和自噬之间的串扰。自噬可以通过各种途径调节细胞对铁死亡的敏感性。Erastin、artesunate、MON-P53和Cys将铁死亡与细胞凋亡密切相关。ELAVL1通过与 BECN1 mRNA 3'-非翻译区 F3 内富含 AU 的元件结合来促进自噬。BECN1可以通过直接阻断System xc-促进铁死亡。
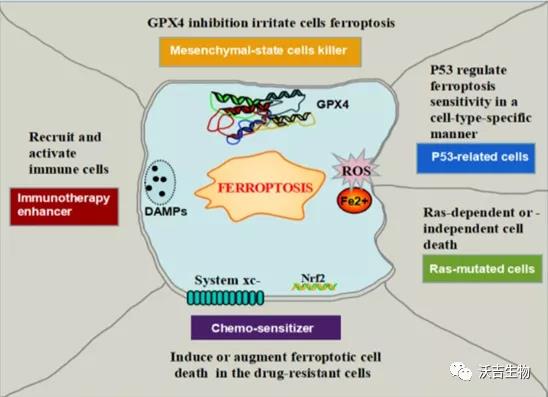
铁死亡可以作为杀死间充质状态细胞的新型细胞死亡或作为免疫疗法和化学疗法的重要协同剂。P53以细胞类型特殊的方式调节铁死亡敏感性。大量小分子和药物以Ras依赖性或非依赖性方式调节铁死亡。
05.沃吉相关产品
名称:细胞铁死亡PCR阵列(Ferroptosis PCR Array)
货号:wc-mRNA0271(人、大小鼠,及接受定制)
货期:人、大小鼠五个工作日、定制请咨询

基因列表:
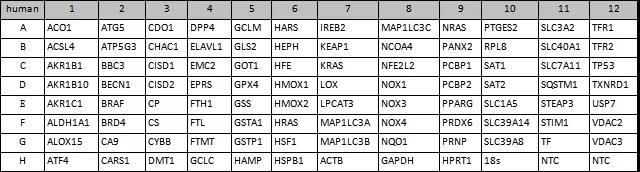

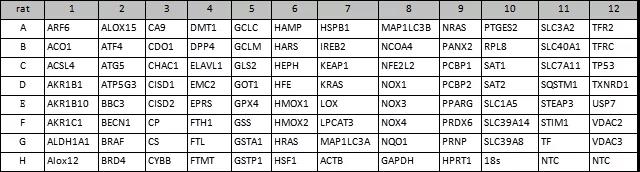
参考文献:Mou Y, Wang J, Wu J, He D, Zhang C, Duan C, Li B. Ferroptosis, a new form of cell death: opportunities and challenges in cancer. J Hematol Oncol. 2019 Mar 29;12(1):34. doi: 10.1186/s13045-019-0720-y. PMID: 30925886; PMCID: PMC6441206.
不感兴趣
看过了
取消

人点赞

人收藏

打赏
不感兴趣
看过了
取消






您已认证成功,可享专属会员优惠,买1年送3个月!
开通会员,资料、课程、直播、报告等海量内容免费看!

打赏金额
认可我就打赏我~
1元 5元 10元 20元 50元 其它
打赏作者
认可我就打赏我~
扫描二维码
立即打赏给Ta吧!
温馨提示:仅支持微信支付!
已收到您的咨询诉求 我们会尽快联系您
