明确肠道菌群在AD发病机制和病情进展中的地位和作用,可为AD预防和治疗提供新的策略和思路。
越来越多的研究证据显示,肠道微生物群与阿尔茨海默病(AD)的产生和进展直接相关。肠道微生物及其代谢产物通过肠-脑轴影响大脑,促进AD患者神经和认知功能的改变,并涉及神经系统、内分泌系统和免疫系统等多种交流途径,这为AD患者的早期识别诊断提供了新的研究思路。
肠道微生物的影响因素众多,包括年龄、情绪、生活和用药方式等,通过早期健康干预(如生活方式干预)调节肠道微生物多样性从而改善AD患者的临床症状,为未来AD预防和治疗研究开辟了一个新的方向。
01
阿尔茨海默症(AD)患者肠道菌群发生显著改变
越来越多研究表明,肠道菌群的组成和功能可影响年龄相关性认知障碍和痴呆的病理生理,也再次证明了肠道菌群的改变可能是阿尔茨海默病发病的原因之一。
2021年,美国健康中心发表了一篇文章,介绍了肠道菌群影响AD相关大脑功能的作用机制。

每个人的肠道菌群都是独一无二的,肠道菌群的多样性和丰度变化将伴随一生,在20-60岁的成人阶段,肠道菌群是高度稳定的,然而,在生命初期和老年期,肠道菌群的组成截然不同,一旦出现菌群失衡,就会影响神经系统发育。

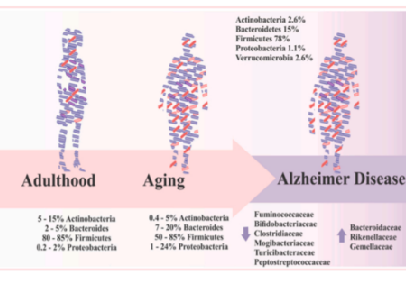
图:不同年龄段和AD患者肠道菌群组成的变化
成年人肠道菌群以厚壁菌门为主,拟杆菌门第二,放线菌门第三,厚壁菌门/拟杆菌门比值为10.9;
大部分老年人群中,拟杆菌门占大部分,其次是厚壁菌门,厚壁菌门/拟杆菌门比值降至0.6;
AD患者肠道菌群瘤胃球菌科、双歧杆菌科、梭菌科、Turicibacteraceae、消化链球菌科较少;拟杆菌科、理研菌科和Gemellaceae 较多。
肠道菌群在老年群体中的显著变化与AD的发生密不可分,了解老年人的基线肠道菌群谱有助于研究肠道菌群参与影响AD发生的机制,肠道菌群的变化可能预示着AD的早期阶段。
另外,在关于阿尔茨海默病患者与健康对照组的肠道菌群特征中研究发现:
在年龄、性别、体质指数等方面的特征无显著性差异情况下,对比发现:认知障碍和脑淀粉样变性患者的肠道菌群中,促炎菌埃希氏菌/志贺氏菌数量增加,而抗炎菌大肠杆菌数量减少。
在年龄、性别和病史方面没有显著差异时,发现阿尔茨海默病患者粪便中能够合成丁酸盐的菌群比例下降,促炎菌的丰度增加了。
许多研究表明,
。
02
"微生物-肠-脑轴"在阿尔茨海默症(AD)发病机制中的作用
2020年,吉林大学第一医院在分子神经生物学期刊上发表了一篇综述,概述了肠道菌群失调对AD的影响。

肠道菌群与大脑之间可以独立运转又相互协同,通过代谢、内分泌、神经和免疫等途径进行双向交流。
肠道菌群代谢物(如短链脂肪酸等)可以到达大脑,实现神经调节功能;
肠道菌群与下丘脑-垂体-肾上腺轴相互作用,调节肾上腺皮质激素或皮质酮激素等,调节大脑功能和肠道菌群组成;
迷走神经的直接激活,可以将肠道菌群对各种刺激做出的各种反应信息传递到大脑,从而影响大脑功能;
脂多糖(LPS)等肠道菌群代谢产物可以激活外周免疫系统和中枢神经系统,介导多种神经生理过程,包括维持血脑屏障完整性、神经发育、神经传递和中枢神经系统免疫激活。

图:微生物-肠-脑轴在AD发病机制中的作用
肠道菌群失调导致菌群代谢异常,乙酸、丙酸、丁酸等有益短链脂肪酸减少,致使有害物质趁虚而入,破坏肠黏膜屏障和血脑屏障,激活外周免疫反应,诱发神经炎症、增加淀粉样斑块形成,从而促进AD疾病进展。
因此,"微生物-肠-脑轴"对维持大脑稳态至关重要,肠道菌群通过代谢、内分泌、神经和免疫途径与大脑连接起来。肠道菌群失调可能会加剧AD发展过程中的淀粉样蛋白聚集和神经炎症。
03
肠道菌群的组成与阿尔茨海默症(AD)发病机制的关系
泰国清迈大学和印度阿拉加帕大学,在2020年发表了一篇总结肠道菌群与AD发病机制的文章。

外在因素(饮食、生活方式、感染)和内在因素(遗传、代谢物、免疫反应和激素)都会影响肠道菌群的组成,进而影响产生的神经递质或代谢产物(胆碱、色氨酸、短链脂肪酸)等。肠道菌群组成的改变会促进脂多糖(LPS)和淀粉样蛋白的释放,导致AD的发生发展。

图:肠道菌群和AD发病机制的关系
随着年龄的增长,肠道菌群结构的变化可能会导致促炎菌增多和抗炎菌减少,从而诱发全身和局部的炎症反应。这种炎症状态不仅会增加胃肠道的通透性,还可能损害血脑屏障的功能,进一步加剧神经炎症和神经元的损伤。
当胃肠道上皮和血脑屏障通透性增加时,脂多糖(LPS)和淀粉样蛋白等有害物质能够通过受损的肠道屏障或血脑屏障进入大脑,触发更多的炎症反应和神经元损伤。这种过程加剧了AD的病理进程,使得神经元受到更多的损伤,甚至导致神经元的死亡。
因此,维护肠道菌群的健康平衡对于预防和治疗AD具有重要的意义,未来的研究将进一步揭示肠道菌群与AD之间的复杂关系,为AD的防治提供新的策略和方法。
04
肠道菌群介导阿尔茨海默症(AD)的多种炎症通路
2021年7月,上海交通大学发表了最新的综述,系统性地阐述了肠道菌群通过多种炎症途径在AD的发展中发挥关键作用。

图:AD中肠道菌群通过炎症途径的机制
在AD患者的肠道中,肠道菌群的结构发生了显著变化,这种变化表现为促炎菌的增多和抗炎菌的减少,这直接导致了肠道内促炎性成分。如LPS(脂多糖)、淀粉样蛋白和支链氨基酸的产生增加。同时,抗炎代谢产物,如短链脂肪酸、胆汁酸和神经递质等的减少,进一步加剧了肠道的炎症状态。
这些肠道内的变化并不孤立存在,它们通过"微生物-肠-脑"轴与大脑紧密相连。具体来说,肠道炎症可以通过神经、内分泌和免疫等多种途径影响大脑,加剧AD的病理进程。其中,神经炎症是这一过程中的关键环节,神经炎症不仅促进了β淀粉样蛋白的产生,还增加了Tau蛋白的聚集和神经元的损伤,从而加剧了AD的症状。
值得注意的是,炎症在AD的发病机制中起着至关重要的作用。除了神经炎症外,全身炎症也是AD发展的重要推动因素。这种全身炎症可能与肠道菌群的失衡密切相关,因为肠道菌群可以通过多种途径影响全身的免疫系统,从而引发全身炎症。
小结:
在衰老的过程中,人体的肠道菌群、免疫系统和肠道黏膜屏障、血脑屏障、"微生物-肠-脑"轴都在发生变化,肠道菌群组成、代谢产物的改变以及与之相关的机体炎症状态,激活神经免疫-炎症反应,β淀粉样蛋白生成增加、tau蛋白过度磷酸化,从而诱导并加重AD。明确肠道菌群在AD发病机制和病情进展中的地位和作用,可为AD预防和治疗提供新的策略和思路。
不感兴趣
看过了
取消

人点赞

人收藏

打赏
不感兴趣
看过了
取消






您已认证成功,可享专属会员优惠,买1年送3个月!
开通会员,资料、课程、直播、报告等海量内容免费看!

打赏金额
认可我就打赏我~
1元 5元 10元 20元 50元 其它
打赏作者
认可我就打赏我~
扫描二维码
立即打赏给Ta吧!
温馨提示:仅支持微信支付!
已收到您的咨询诉求 我们会尽快联系您
